La detección precoz del embolismo aéreo venoso (EAV) durante las intervenciones neuroquirúrgicas en sedestación disminuye la gravedad de sus complicaciones.
ObjetivosAnalizar la detección de EAV y sus repercusiones en pacientes intervenidos en sedestación. Comprobar la frecuencia de aspiración de aire a través de una vía venosa central. Valorar la viabilidad del uso del Doppler transcraneal (DTC) en quirófano para el diagnóstico del foramen oval permeable (FOP).
Material y métodosEstudio prospectivo de intervenciones neuroquirúrgicas consecutivas realizadas durante 5 años en sedestación. Como método diagnóstico del EAV se empleó el Doppler precordial y el CO2 espirado. El FOP se exploró tras la inducción anestésica mediante DTC.
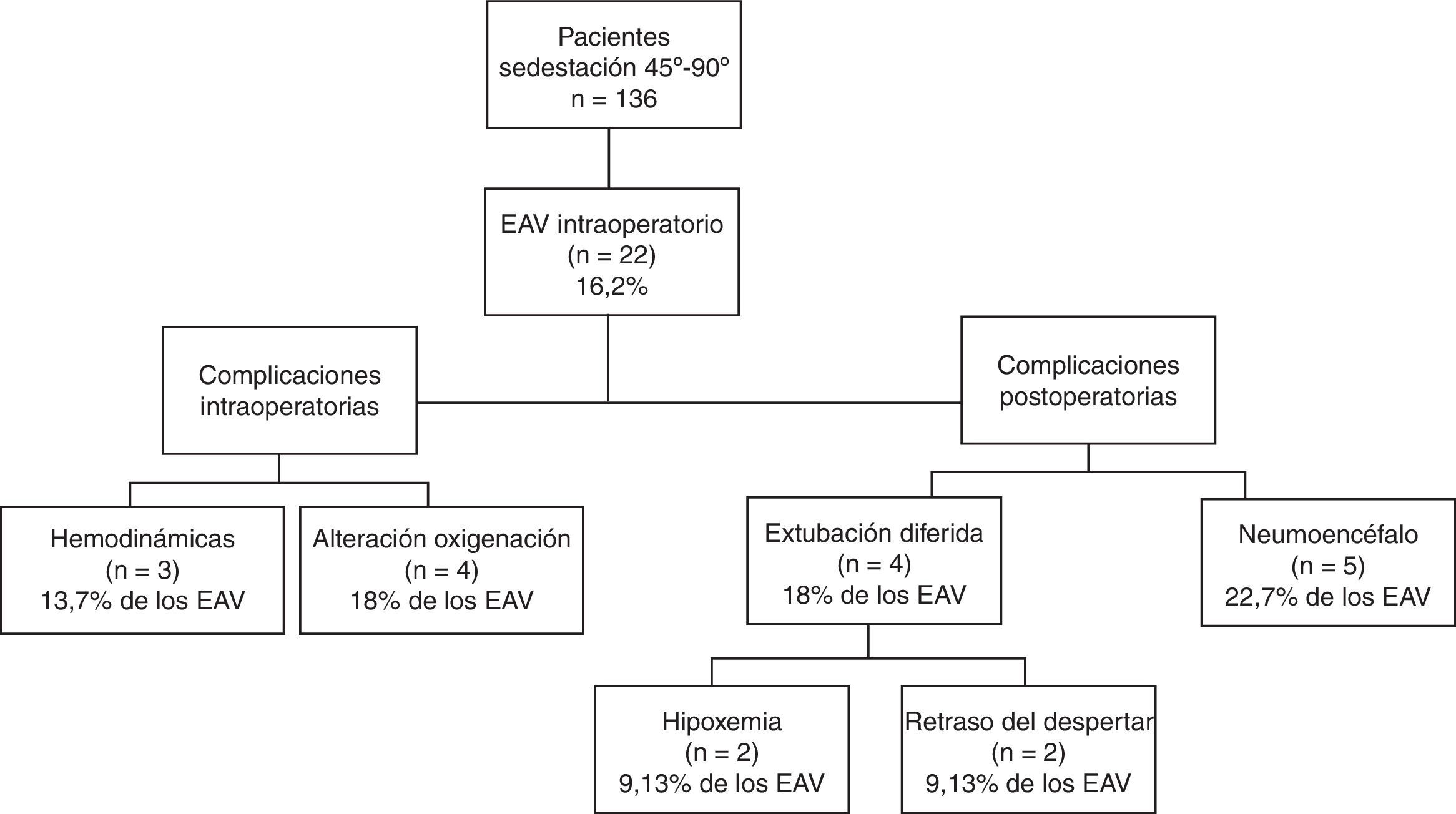
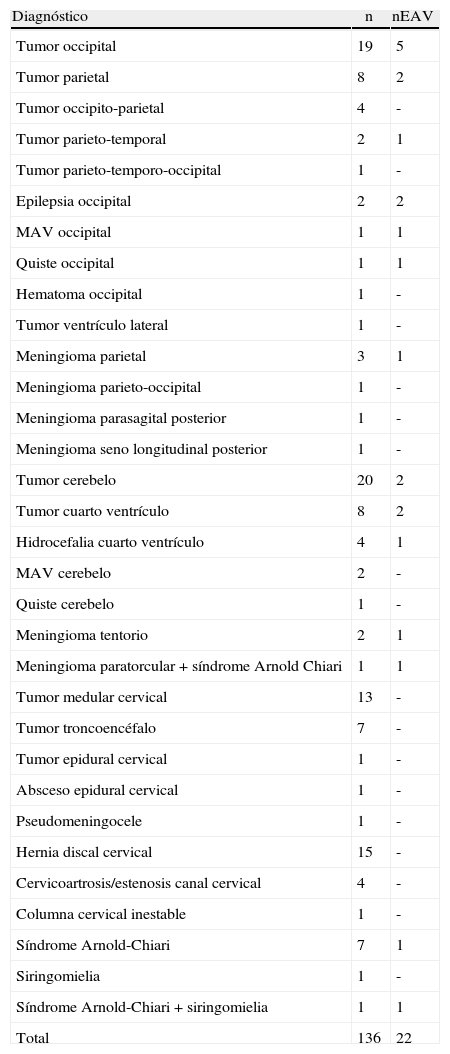
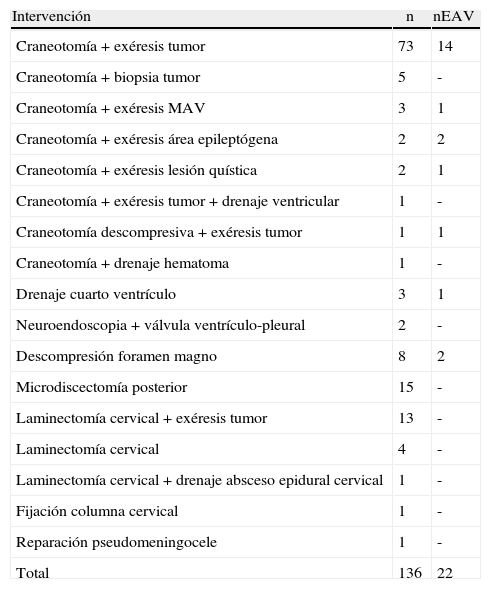
ResultadosCiento treinta y seis pacientes fueron intervenidos en sedestación, 93 craneotomías y 43 cirugías de columna cervical. Veintidós pacientes (16,2%) fueron diagnosticados de EAV (21,5% de las craneotomías y 4,7% de las cirugías de columna; p=0,013). En el 59% de los casos se aspiró aire a través del catéter venoso central. Hubo afectación hemodinámica en 3 pacientes, alteración de la oxigenación en 4 y neumoencéfalo clínicamente relevante en 5. Dos pacientes (1,4%) fueron diagnosticados de FOP, pero no presentaron episodios de EAV ni embolia aérea paradójica.
ConclusionesConfirmamos una mayor incidencia de EAV en craneotomías que en cirugía de columna cervical en sedestación. Obtuvimos aire a través del catéter venoso central en más de la mitad de los casos. Con nuestra sistemática, ningún paciente presentó complicaciones críticas intraoperatorias. La baja incidencia de FOP detectada con DTC requerirá modificar nuestro protocolo realizado con el paciente anestesiado.
Early detection of venous air embolism (VAE) during neurosurgical procedures in sitting position decreases the severity of its complications.
Objectivesour aim was to analyse the detection of VAE and its impact on patients operated in a sitting position, verify air aspiration through a central venous catheter and assess the feasibility of the routine use of transcranial Doppler (TCD) for intraoperative diagnosis of patent foramen ovale (PFO).
Material and methodsWe performed a prospective study of consecutive neurosurgical procedures performed in the sitting position for 5 years. Precordial Doppler and end-tidal carbon dioxide were the diagnostic methods for VAE. PFO was explored by TCD after anaesthetic induction.
Results136 patients were operated in the sitting position, 93 craniotomies and 43 cervical spine procedures. Twenty-two patients (16.2%) were diagnosed with VAE (21.5% of craniotomies and 4.7% of spinal surgeries; p=.013). In 59% of cases, air was aspirated through the central venous catheter. There was haemodynamic involvement in 3 patients, impaired oxygenation in 4 and clinically relevant pneumocephalus in 5 of them. Two patients (1.4%) were diagnosed with PFO, but did not present episodes of VAE or paradoxical air embolism.
ConclusionsThe series analysed confirmed a higher incidence of VAE in craniotomies than in cervical spine surgery in a sitting position. We were able to aspirate air through the central venous catheter in more than half the cases. No patients suffered critical intraoperative complications following our approach. The low incidence of PFO detected with TCD will imply a modification of our protocol performed on anaesthetised patients.
Artículo

Si es la primera vez que accede a la web puede obtener sus claves de acceso poniéndose en contacto con Elsevier España en suscripciones@elsevier.com o a través de su teléfono de Atención al Cliente 902 88 87 40 si llama desde territorio español o del +34 932 418 800 (de 9 a 18h., GMT + 1) si lo hace desde el extranjero.
Si ya tiene sus datos de acceso, clique aquí.
Si olvidó su clave de acceso puede recuperarla clicando aquí y seleccionando la opción "He olvidado mi contraseña".
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora