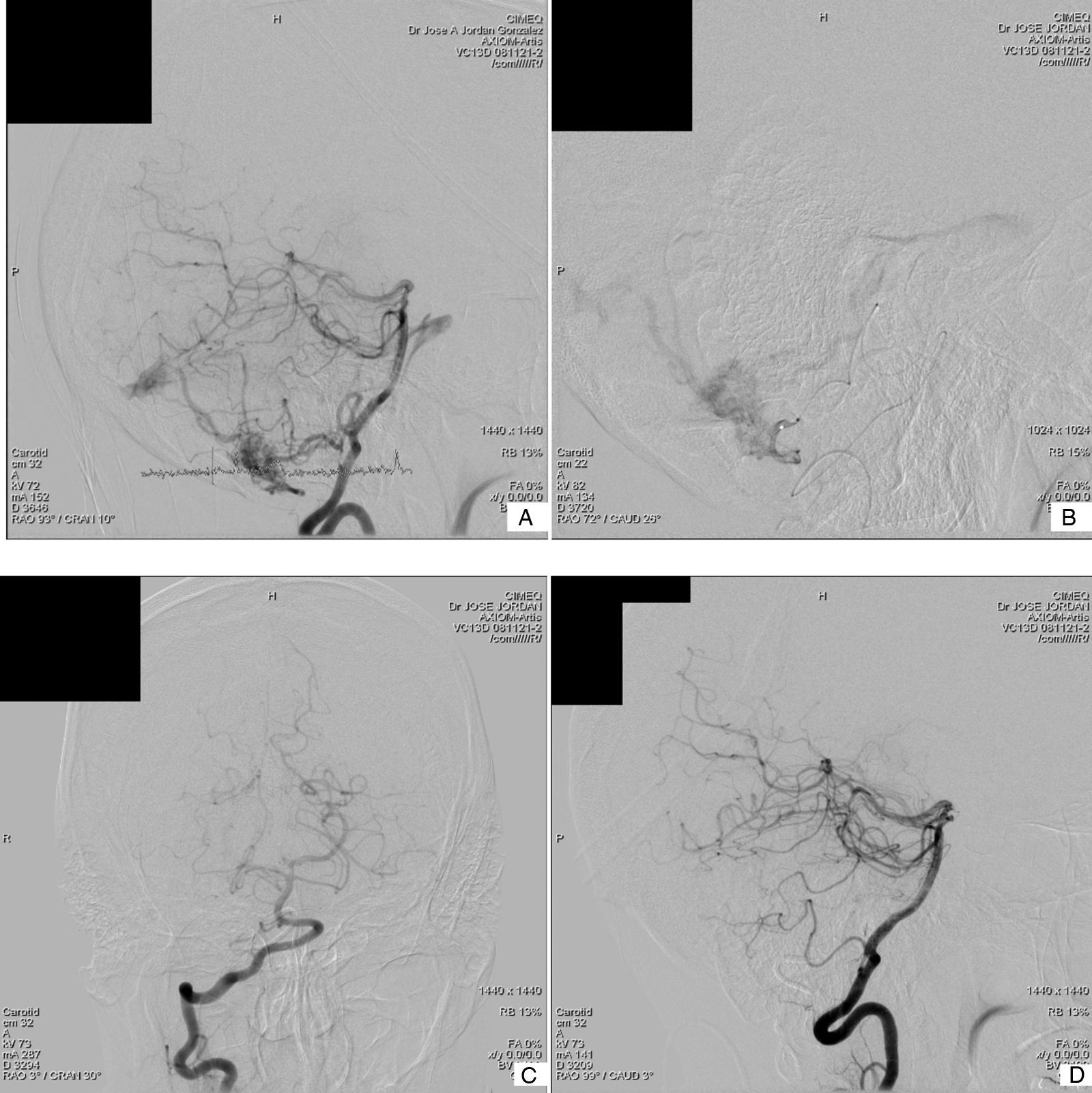
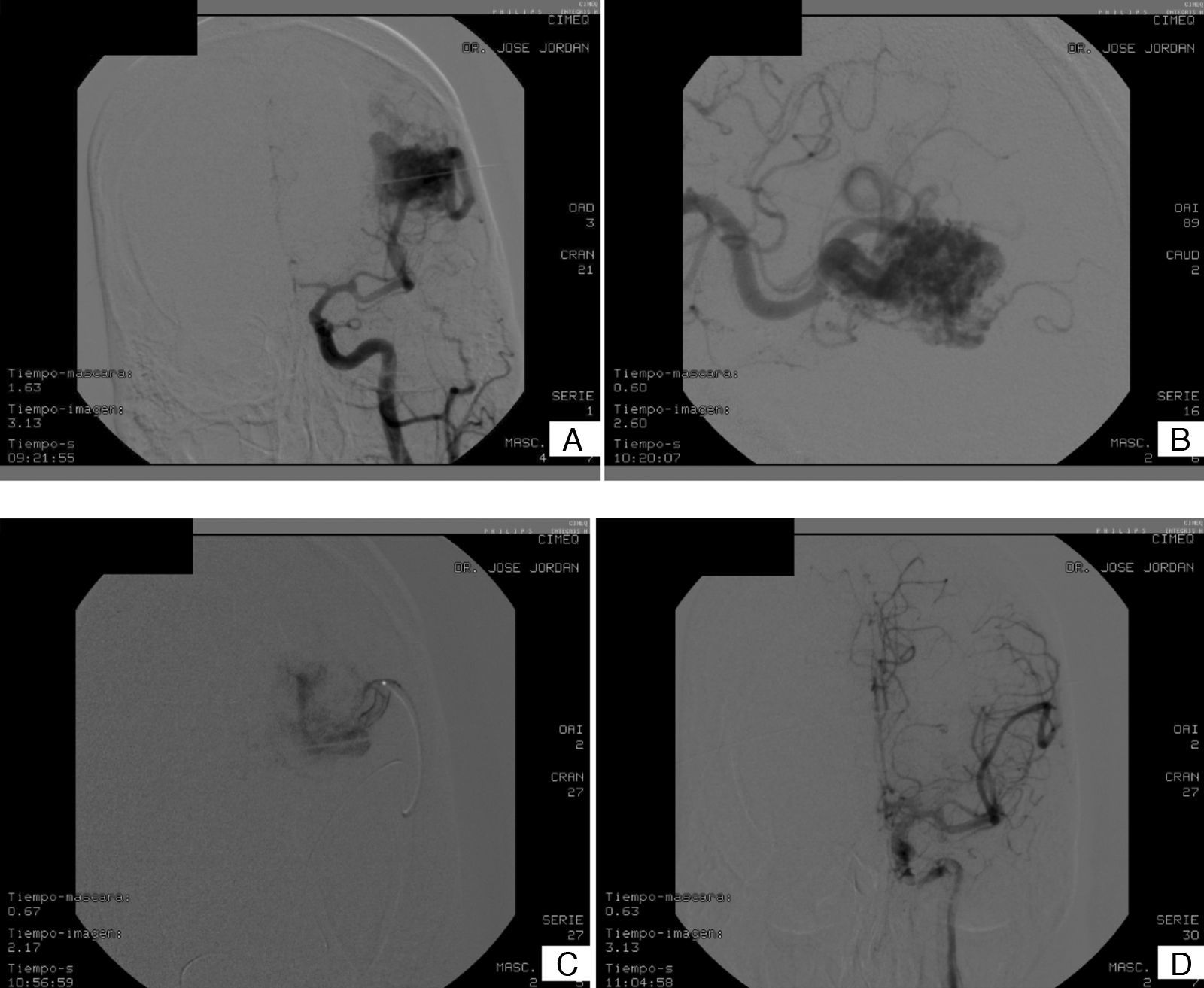
Las malformaciones arteriovenosas (MAV) constituyen malformaciones vasculares del sistema nervioso central, responsables de una morbimortalidad significativa. La embolización con n-butil cianoacrilato es una modalidad de tratamiento bien establecida que se combina con la cirugía o la radiocirugía. Nuestro objetivo, en este trabajo, fue caracterizar la serie de MAV tratadas por vía endovascular con n-butil cianoacrilato en la población cubana y evaluar los resultados postembolización.
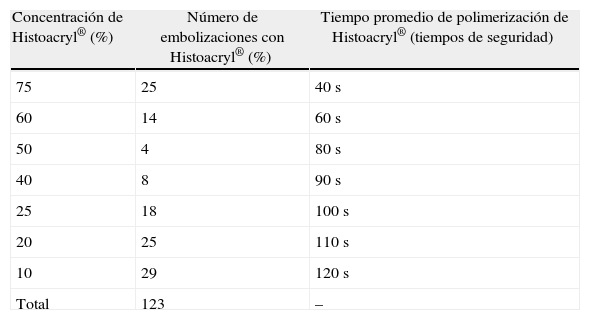
Material y métodoUn total de 58pacientes con MAV cerebrales fueron embolizados con n-butil cianoacrilato en la unidad de terapia endovascular del Centro de Investigaciones Médico Quirúrgicas (CIMEQ) en la Habana (Cuba) en el quinquenio comprendido entre febrero de 2006 y febrero de 2011. Se realizaron un total de 91sesiones que comprendieron embolizaciones intranidales y desvascularizaciones predominantemente parciales, de un 25-30% por sesión, y cierre de 123pedículos arteriales. Se establecieron tiempos de seguridad para la inyección del n-butil cianoacrilato mediante el cálculo de su tiempo de polimerización, utilizando sistemáticamente la hipotensión postembolización y la realización de test superselectivo con propofol para la determinación de elocuencia cerebral.
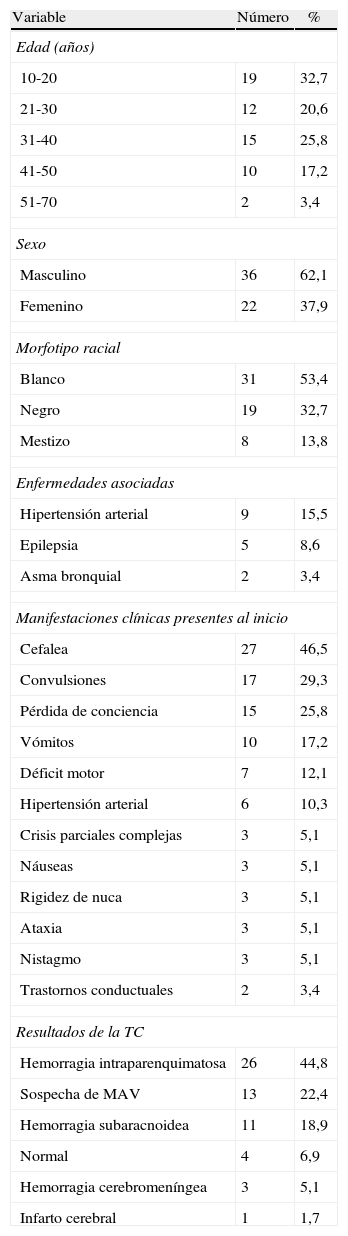
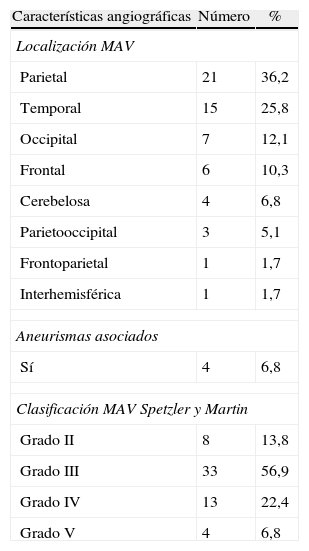
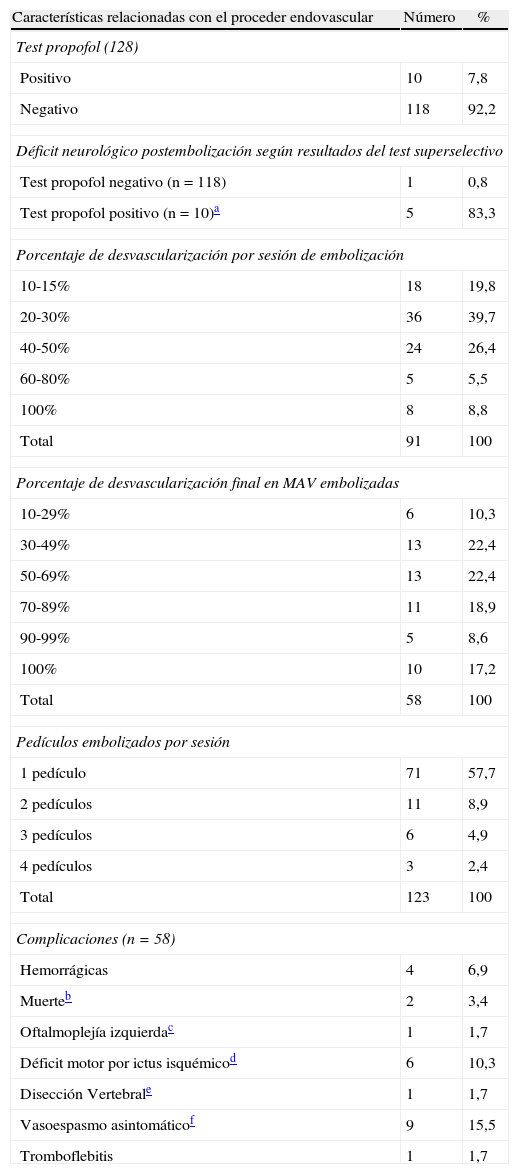
ResultadosEl 68,8% de los casos empezaron con manifestaciones hemorrágicas, el 24,1% con crisis epilépticas y el 1,7% con ictus isquémico. El 93,2% de las MAV fueron supratentoriales y el 6,8%, infratentoriales; según la clasificación de Spetzler y Martin, el 13,8% eran de grado ii, el 56,9% de grado iii, el 22,4% de grado iv y el 6,8% de grado v. Se realizaron 128tests superselectivos con propofol, 118 (92,2%) negativos y 10 (7,8%) positivos. Predominaron las desvascularizaciones parciales del 20-30%; en el 17,2% de los pacientes se logró oclusión total, y en el 27,5%, del 70-99%. Se establecieron tiempos de seguridad para la inyección de Histoacryl®, y se estableció la utilización de la hipotensión posprocedimiento. Se registró una morbilidad del 17,2%, con un 6,9% de complicaciones hemorrágicas y una mortalidad del 3,4%.
ConclusionesLas tasas de oclusión total y de morbimortalidad se encuentran en los rangos descritos internacionalmente. La implementación de cierres intranidales con desvascularizaciones del 20-30% por sesión y la utilización de la hipotensión posprocedimiento después de las complicaciones hemorrágicas descritas se tradujo en ausencia de complicaciones hemorrágicas.
Arteriovenous malformations (AVMs) constitute malformative lesions of the central nervous system vasculature and cause significant morbidity and mortality. Endovascular embolization with n-butyl cyanoacrylate is a well established modality of AVM treatment, usually combined with surgery or radiosurgery. The purpose of this study was to characterise the AVMs that were treated endovascularly with n-butyl cyanoacrylate and to evaluate the post-embolization results in the Cuban population.
Materials and methodsFrom February 2006 to February 2011, a group of 58 consecutive patients with brain AVMs were embolized using n-butyl cyanoacrylate in the endovascular therapy unit of the Medical Surgical Research Centre in Havana (Cuba). In all, 91sessions were carried out with intranidal embolization and mainly partial devascularization, 25-30% per session, and closing 123 arterial pedicles. Safety times for n-butyl cyanoacrylate injection were established by calculating the polymerisation times for different dilutions, using post-embolisation hypotension systematically, as well as a superselective test with propofol to determine cerebral eloquence.
ResultsHaemorrhagic signs were the initial presentation in 68.8% of the patients, 24.1% presented with epileptic episodes and 1.7% with ischemic stroke. Of the AVMs, 93.2% were supratentorial; according to the Spetzler and Martin classification, 13.8% were grade II, 56.9% were grade III, 22.4% were grade IV and 6.8%, grade V. One hundred and twenty-eight selective tests with propofol were performed and 118 (92.2%) of those were negative. Partial devascularization (20-30%) prevailed; complete obliteration was achieved in 17.2% of the patients and 70%-99% in 27.5% of the patients. Safety times for n-butyl cyanoacrylate injection were established and the use of post-procedure hypotension was settled. Morbidity of 17.2%, with 6.9% haemorrhagic complications and mortality of 3.4% were registered in the whole series.
ConclusionsThe rates of total occlusion and of morbidity and mortality in the series are in the internationally described ranges. The implementation of intranidal closings with 20-30% devascularization per session and the use of post-embolization hypotension after the haemorrhage complications described resulted in the total absence of haemorrhagic complications.
Artículo

Si es la primera vez que accede a la web puede obtener sus claves de acceso poniéndose en contacto con Elsevier España en suscripciones@elsevier.com o a través de su teléfono de Atención al Cliente 902 88 87 40 si llama desde territorio español o del +34 932 418 800 (de 9 a 18h., GMT + 1) si lo hace desde el extranjero.
Si ya tiene sus datos de acceso, clique aquí.
Si olvidó su clave de acceso puede recuperarla clicando aquí y seleccionando la opción "He olvidado mi contraseña".
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora