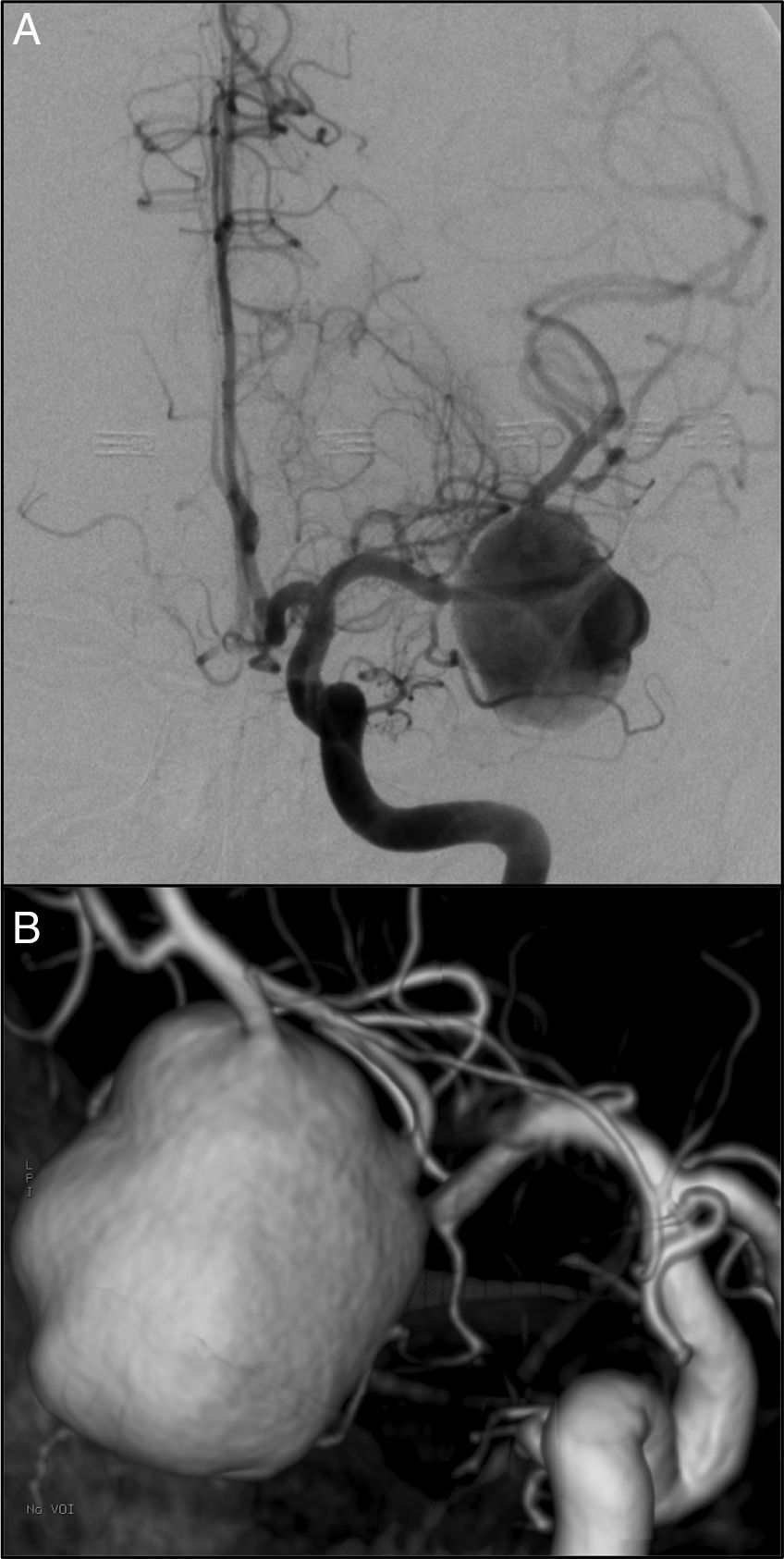
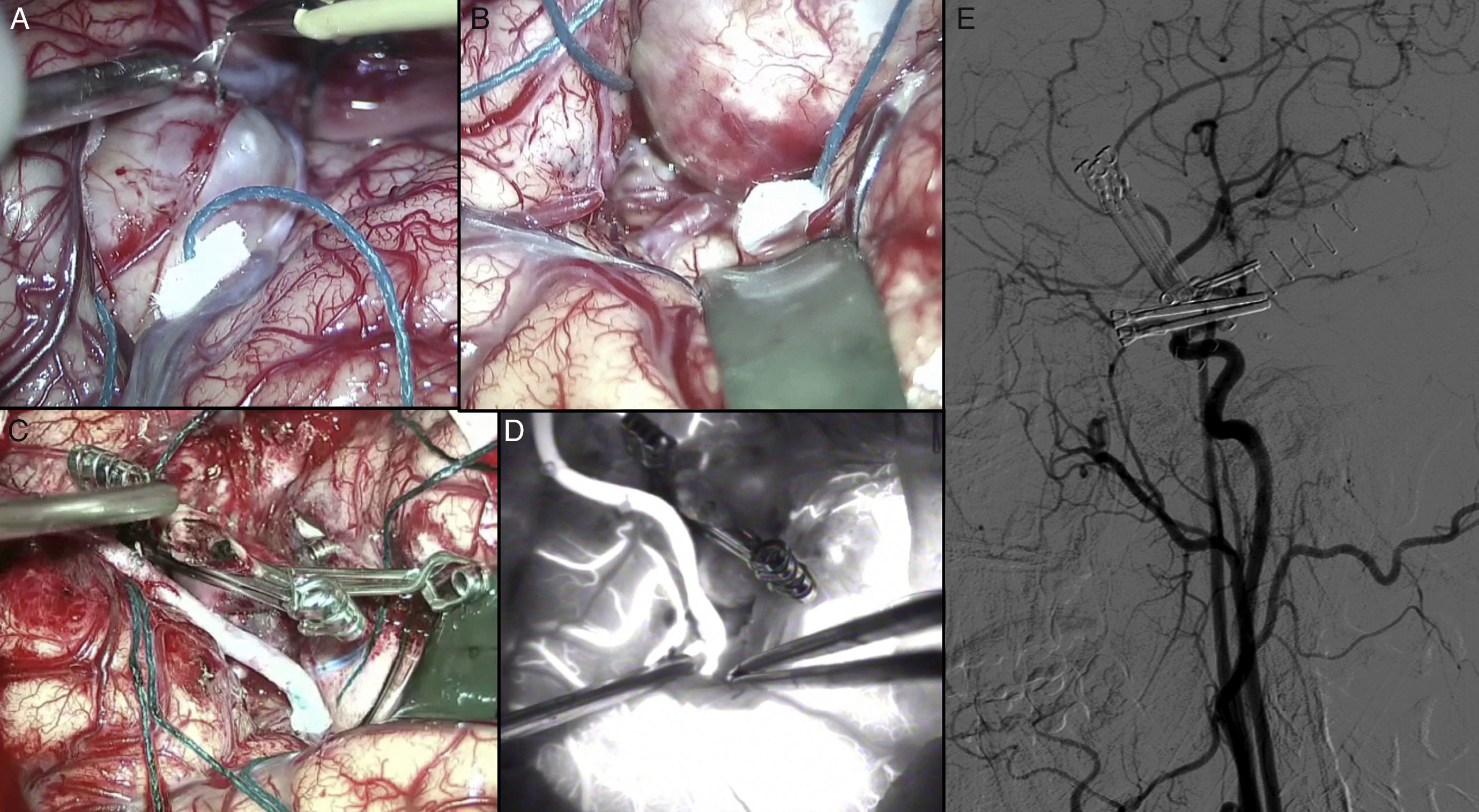
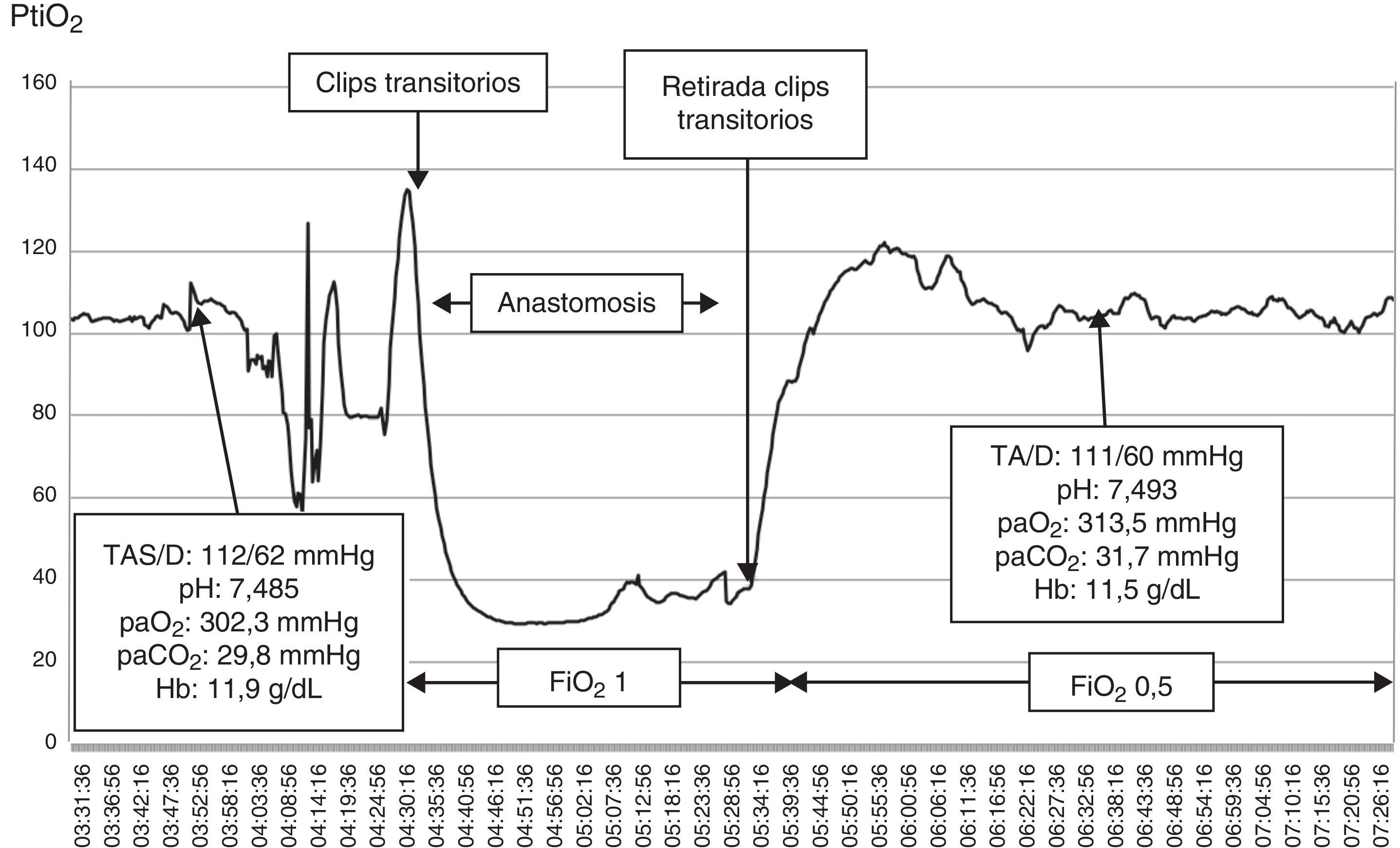
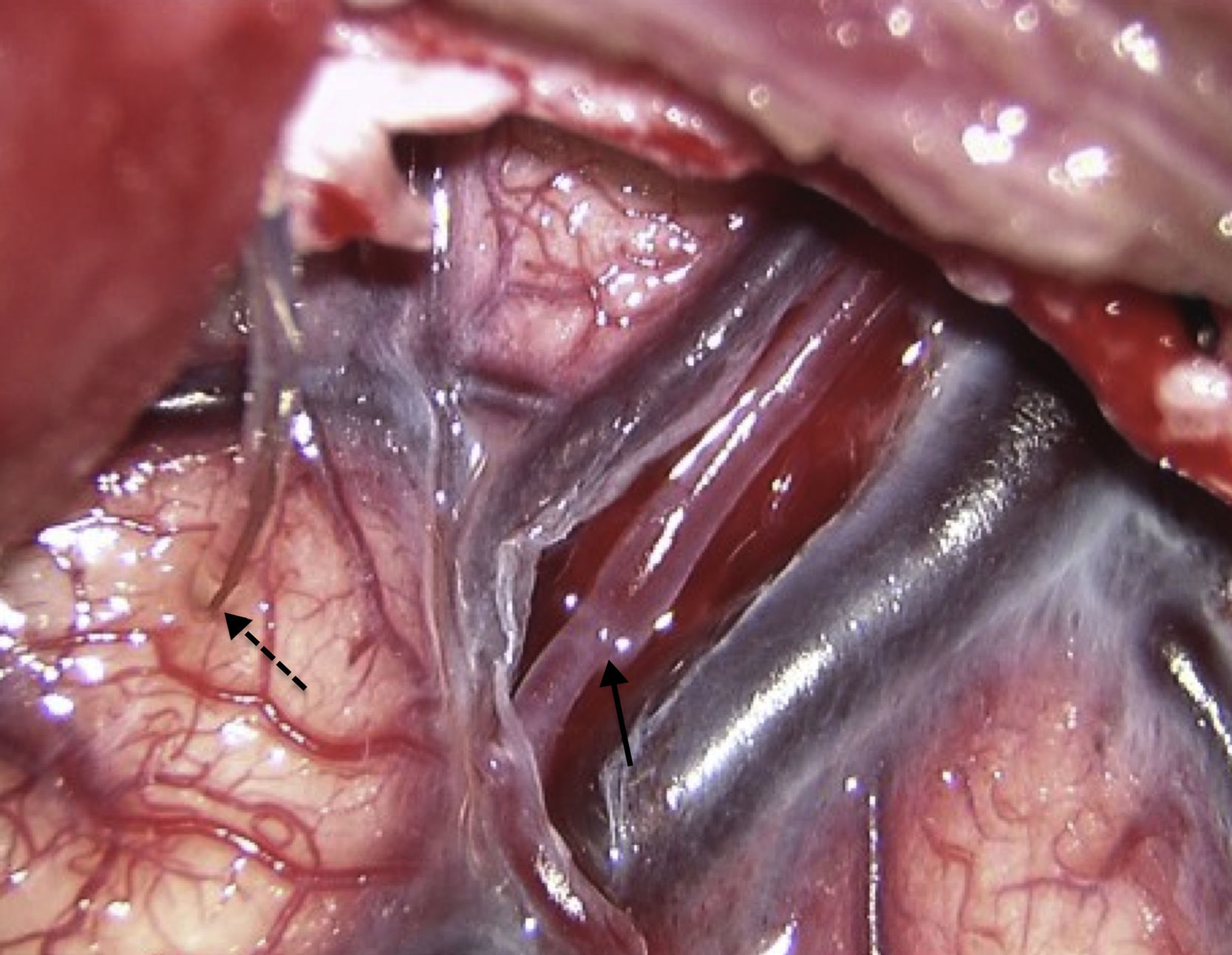
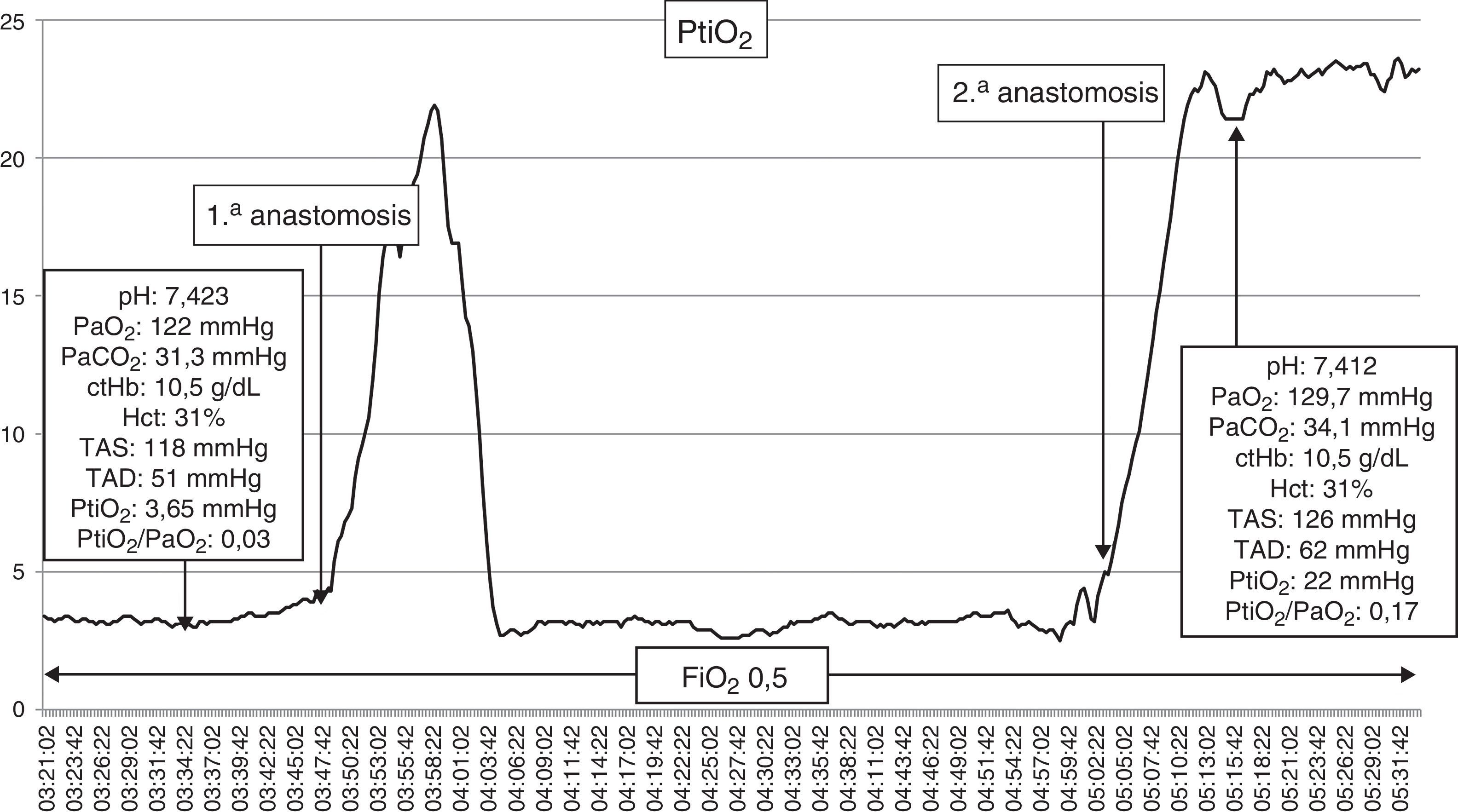
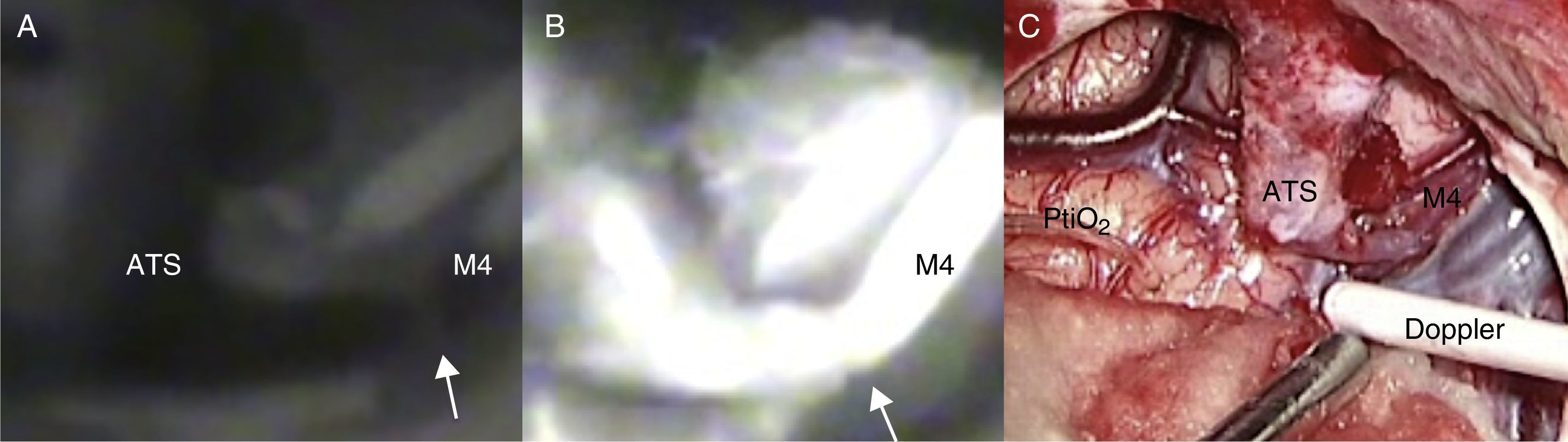
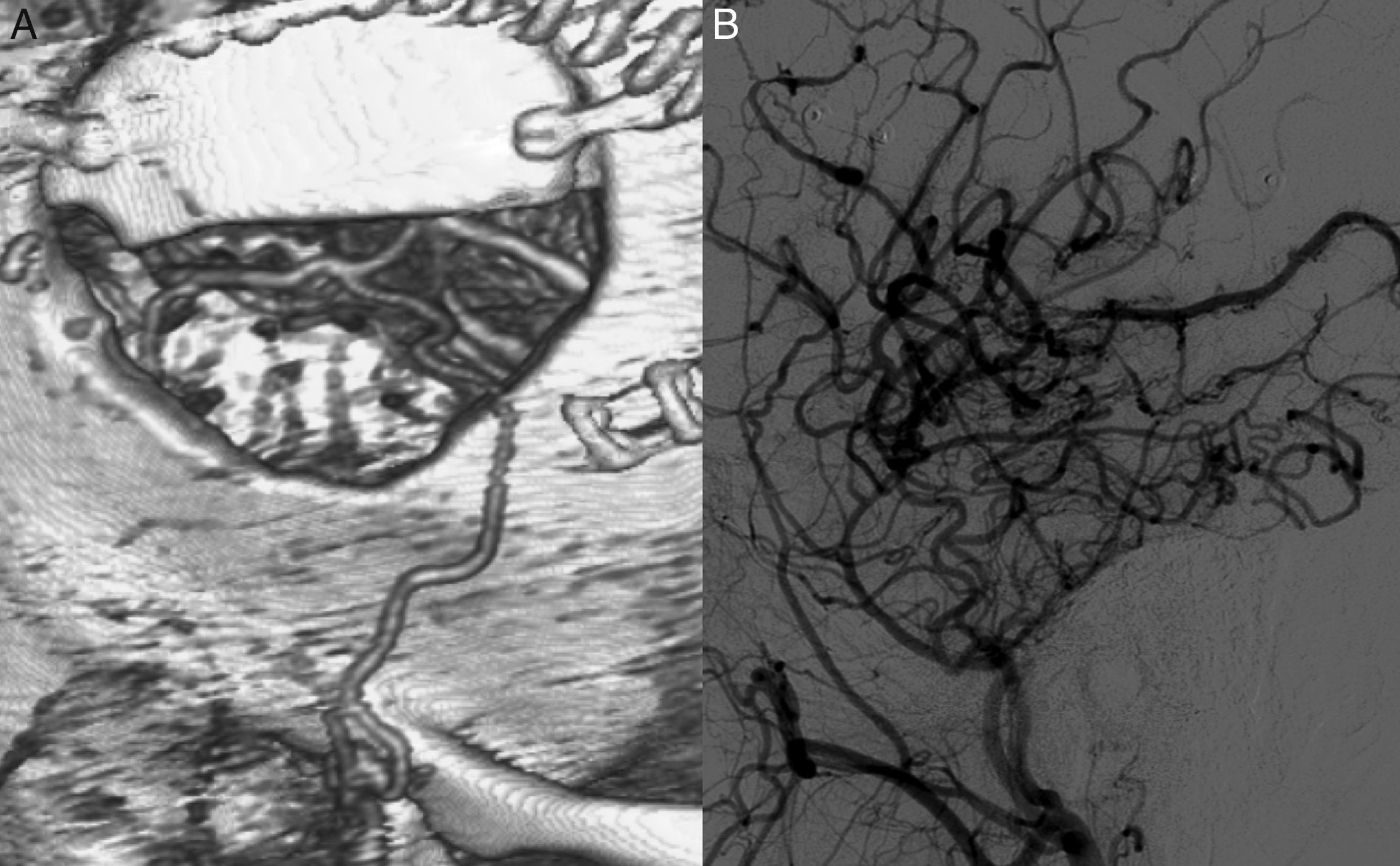
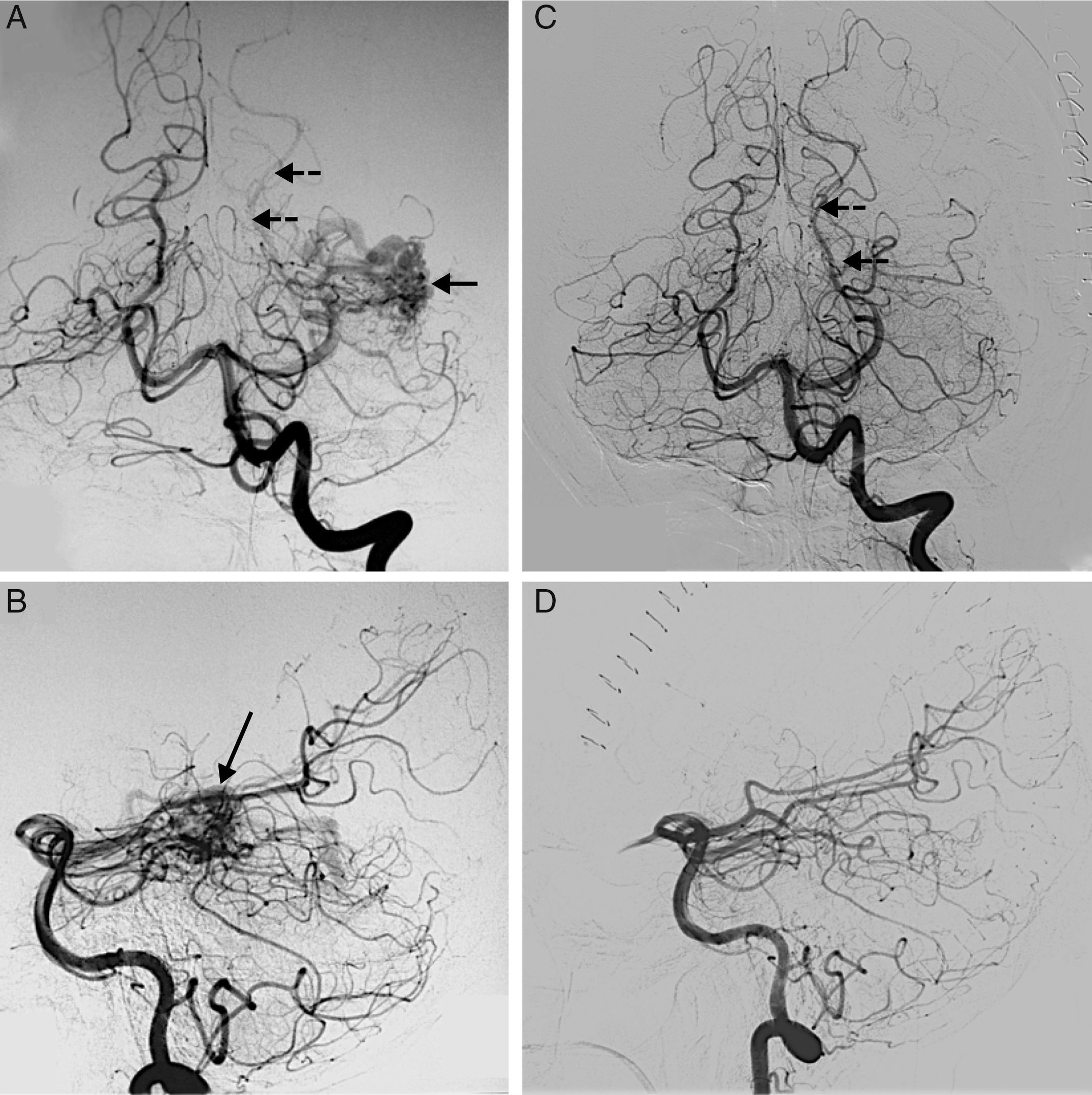
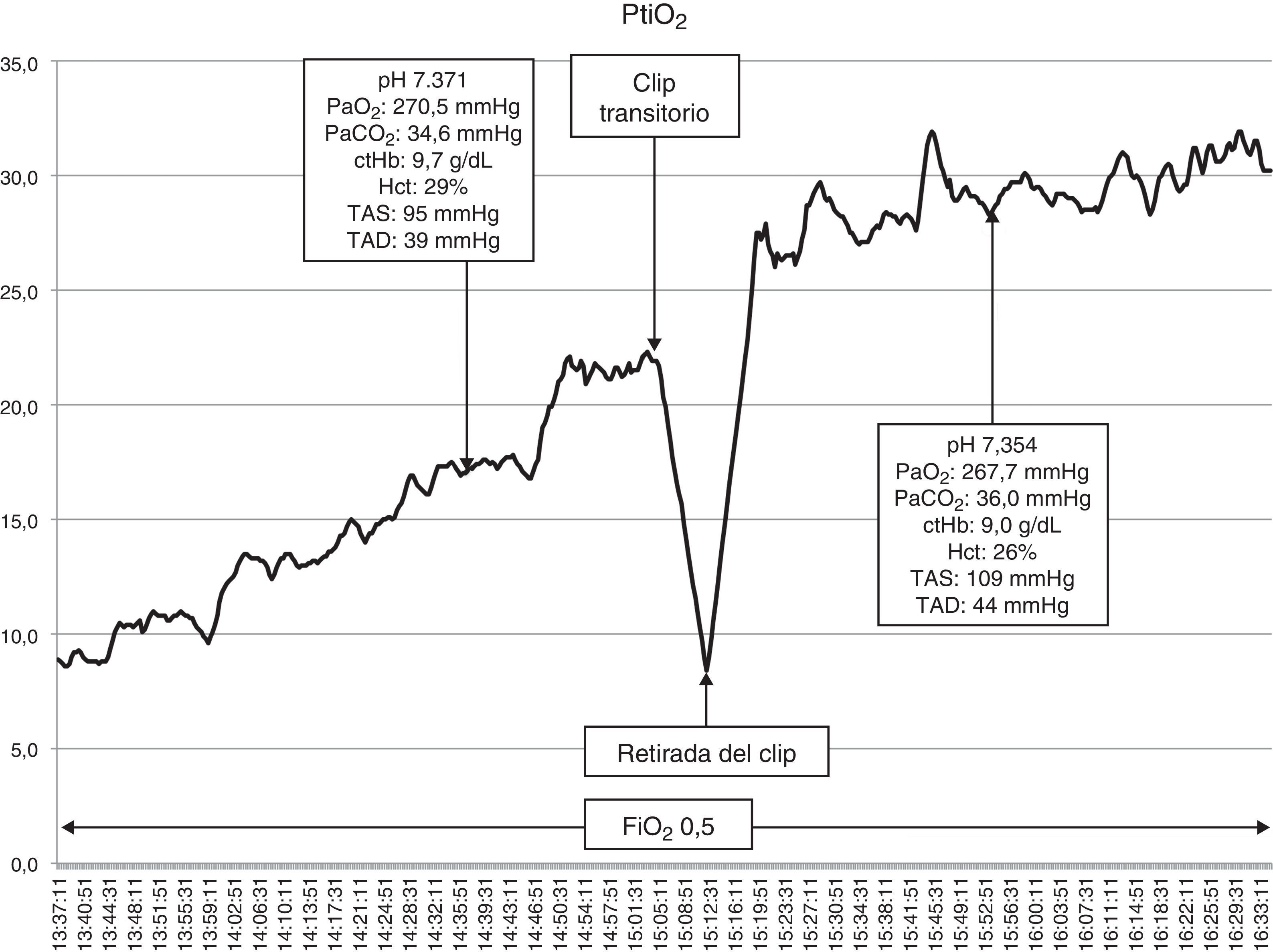
Las lesiones isquémicas relacionadas con los procedimientos quirúrgicos son una de las principales causas de morbilidad en el postoperatorio de la cirugía de los pacientes con patología vascular cerebral. Con el objetivo de detectar intraoperatoriamente los fenómenos isquémicos se han implementado diferentes sistemas de neuromonitorización, entre los que se encuentra la monitorización de la presión tisular de oxígeno (PtiO2). En este trabajo se pretende describir la utilidad de la monitorización intraoperatoria de la PtiO2 en la neurocirugía vascular a partir de la discusión de 4 casos ejemplo. A partir de la presentación de estos casos se discute cómo este tipo de monitorización permite detectar de una forma precoz y fiable las situaciones relacionadas con el procedimiento quirúrgico que ocasionan una hipoxia cerebral isquémica. La monitorización continua de la PtiO2 en el área de riesgo permite además resolver la causa que ha originado los episodios isquémicos y su evolución a un infarto establecido.
Ischemic lesions related to surgical procedures are a major cause of postoperative morbidity in patients with cerebral vascular disease. There are different systems of neuromonitoring to detect intraoperative ischemic events, including intraoperative monitoring of oxygen tissue pressure (PtiO2). The aim of this article was to describe, through the discussion of 4 cases, the usefulness of intraoperative PtiO2 monitoring during vascular neurosurgery. In presenting these cases, we demonstrate that monitoring PtiO2 is a reliable way to detect early ischemic events during surgical procedures. Continuous monitoring of PtiO2 in an area at risk allows the surgeon to resolve the cause of the ischemic event before it evolves to an established cerebral infarction.
Artículo

Si es la primera vez que accede a la web puede obtener sus claves de acceso poniéndose en contacto con Elsevier España en suscripciones@elsevier.com o a través de su teléfono de Atención al Cliente 902 88 87 40 si llama desde territorio español o del +34 932 418 800 (de 9 a 18h., GMT + 1) si lo hace desde el extranjero.
Si ya tiene sus datos de acceso, clique aquí.
Si olvidó su clave de acceso puede recuperarla clicando aquí y seleccionando la opción "He olvidado mi contraseña".