La estimulación medular crónica es una técnica ampliamente aceptada en el tratamiento del dolor lumbar resultante de una cirugía de espalda fallida. Clásicamente la estimulación se ha venido realizando con electrodos percutáneos implantados bajo anestesia local y sedación, sin embargo, la facilidad de migración, así como la dificultad de reproducción de parestesias eléctricas en zonas amplias recogidas con los mismos, han hecho que cada vez más se recurra a la utilización de electrodos planos quirúrgicos, que presentaban como inconveniente la necesidad de una laminectomía y anestesia general para su implantación.
ObjetivosPresentar los resultados clínicos, los detalles técnicos, las ventajas y los beneficios de la implantación de electrodos planos de estimulación medular bajo anestesia espinal, en síndromes de cirugía de espalda fallida.
Material y métodosLa estimulación medular se realizó en un total de 119 pacientes (52 hombres y 67 mujeres), con edades comprendidas entre los 31 y los 73 años (47,3 de media). La anestesia epidural fue inducida con ropivacaína. En todos los casos, a través de una laminectomía mínima, se implantó en el espacio epidural un electrodo plano de 8 contactos o un electrodo plano de moderna generación de 16 polos. La situación definitiva de los electrodos se dispuso en función de la reproducción de parestesias eléctricas en la zona dolorosa de los enfermos. Los electrodos se conectaron con posterioridad a generadores de impulsos eléctricos de doble canal o recargables.
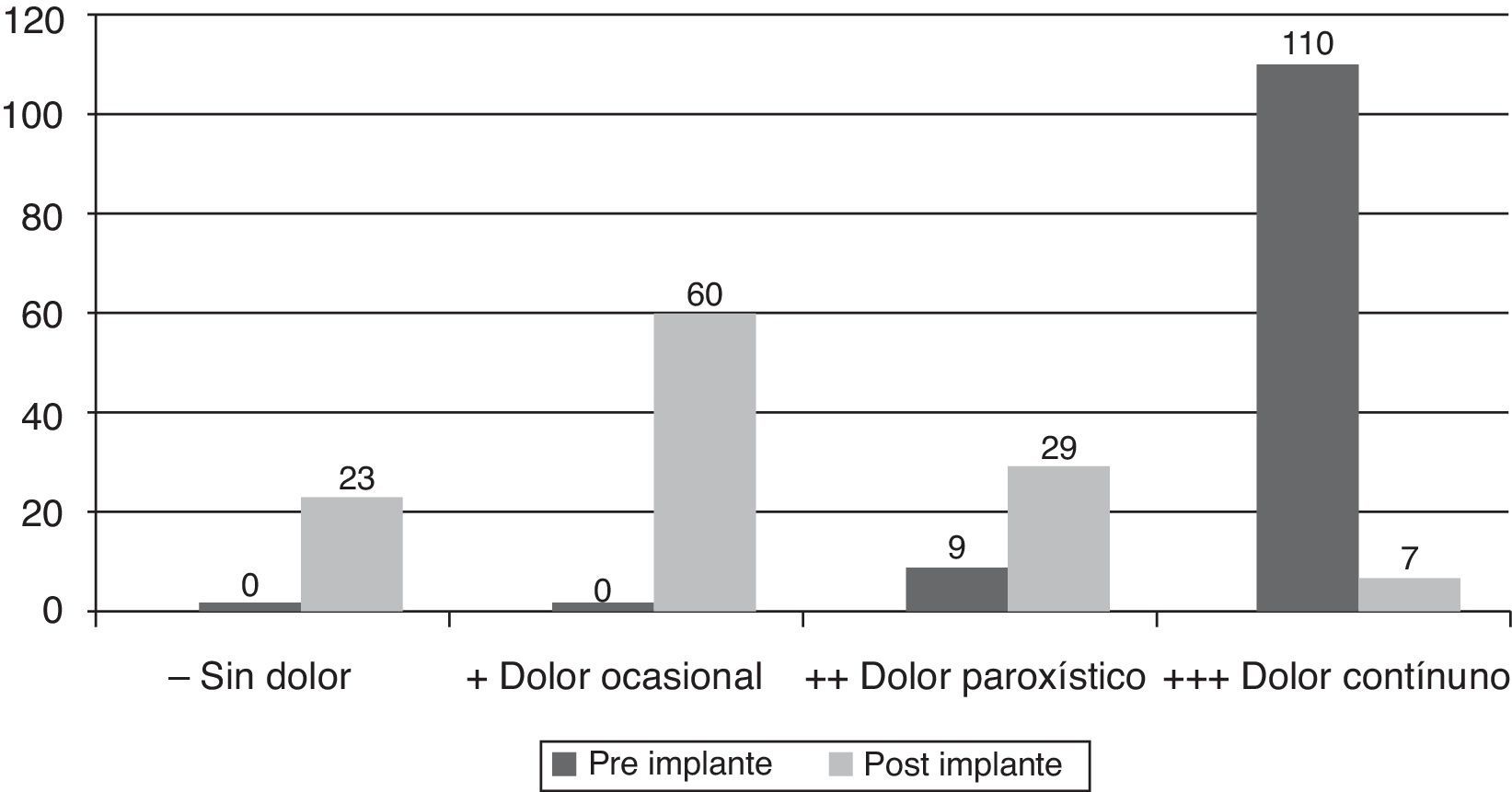
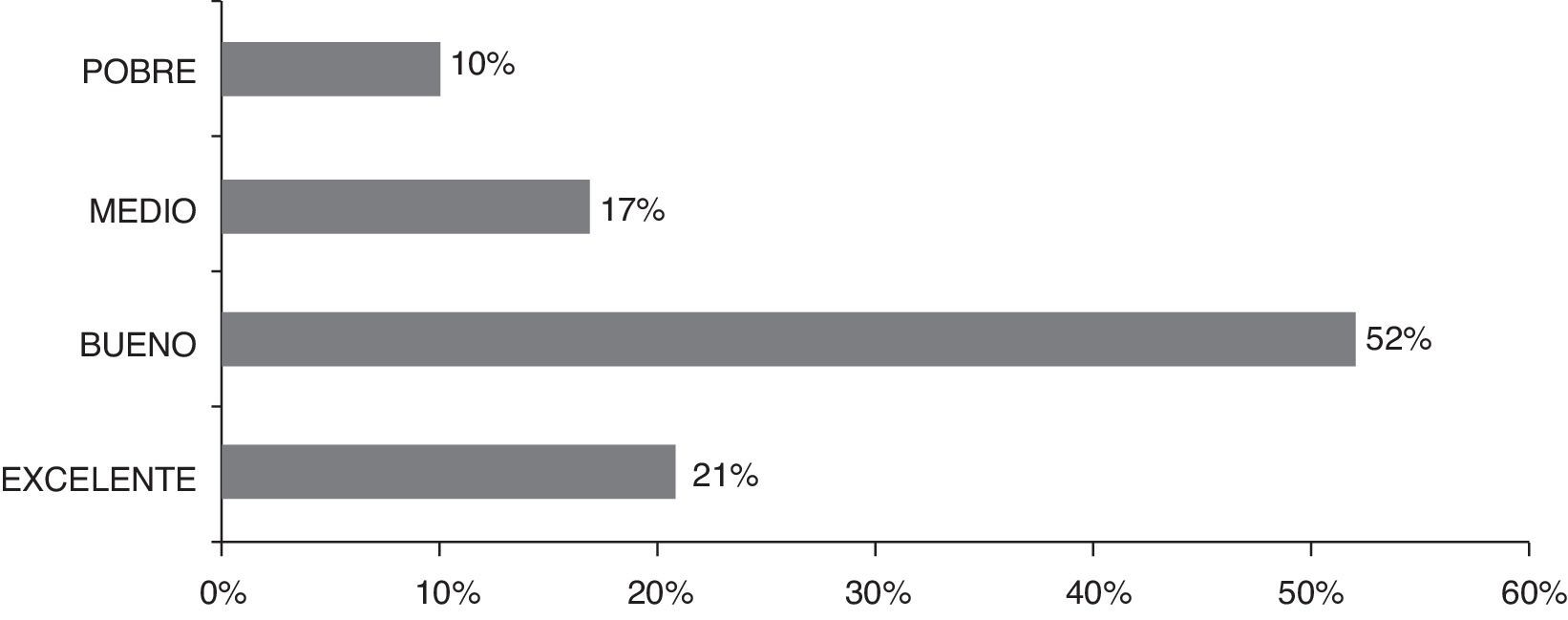
ResultadosDespués de un seguimiento medio de 4,7 años, el resultado en cuanto a la mejoría de la situación dolorosa previa es satisfactorio, constatando una disminución del dolor del 58% en el axial y del 60% en el radicular, en más del 70% de los casos. Ninguno de los pacientes ha manifestado que el tiempo quirúrgico fuera doloroso o desagradable. No se han recogido complicaciones serias en el grupo, y en 6 de los casos se ha tenido que explantar el sistema por ineficacia o intolerancia de la neuroestimulación a largo plazo.
ConclusionesEn este estudio, realizado en un número importante de pacientes, se ha utilizado la anestesia epidural para la colocación de electrodos planos de estimulación medular en síndromes de cirugía fallida de espalda o poslaminectomía. La técnica se ha mostrado segura, eficaz y satisfactoria.
Spinal cord stimulation is a widely-accepted technique in the treatment of back pain resulting from failed back surgery. Classically, stimulation has been carried out with percutaneous electrodes implanted under local anaesthesia and sedation. However, the ease of migration and the difficulty of reproducing electrical paresthesias in large areas with such electrodes has led to increasing use of surgical plate leads, which have the disadvantage of the need for general anaesthesia and a laminectomy for implantation.
ObjectivesOur objective was to report the clinical results, technical details, advantages and benefits of laminectomy lead placement under epidural anaesthesia in failed back surgery syndrome cases.
Material and methodsSpinal cord stimulation was performed in a total of 119 patients (52 men and 67 women), aged between 31 and 73 years (average, 47.3). Epidural anaesthesia was induced with ropivacaine. In all cases we inserted the octapolar or 16-polar lead in the epidural space through a small laminectomy. The final position of the leads was the vertebral level that provided coverage of the patient's pain. The electrodes were connected at dual-channel or rechargeable pulse generators.
ResultsAfter a mean follow-up of 4.7 years, the results in terms of improvement of the previous painful situation was satisfactory, with an analgesia level of 58% of axial pain and 60% of radicular pain in more than 70% of cases. None of the patients said that the surgery stage was painful or unpleasant. No serious complications were included in the group, but in 6 cases the system had to be explanted because of ineffectiveness or intolerance of long-term neurostimulation.
ConclusionsThis study, with a significant number of patients, used epidural anaesthesia for spinal cord stimulation of lead implants by laminectomy in failed back surgery syndromes. The technique seems to be safe and effective.
Artículo

Si es la primera vez que accede a la web puede obtener sus claves de acceso poniéndose en contacto con Elsevier España en suscripciones@elsevier.com o a través de su teléfono de Atención al Cliente 902 88 87 40 si llama desde territorio español o del +34 932 418 800 (de 9 a 18h., GMT + 1) si lo hace desde el extranjero.
Si ya tiene sus datos de acceso, clique aquí.
Si olvidó su clave de acceso puede recuperarla clicando aquí y seleccionando la opción "He olvidado mi contraseña".